Страничка клинициста
Современные возможности прогнозирования послеоперационных осложнений и точного измерения ВГД у пациентов, оперированных методом ЛАСИК (New)
ФГУ «Московский НИИ глазных болезней имени Гельмгольца Росздрава», Москва, Россия
Р Е З Ю М Е
Дана характеристика возможностей нового прибора — Ocular Response Analyzer (ORA), созданного компанией Reichert (США) для измерения роговично–компенсированного внутриглазного давления (ВГД), фактора резистентности роговицы (ФРР) и корнеального гистерезиса (КГ). Вышеуказанные показатели имеют важное значение для оценки биомеханических свойств роговицы, как при различных ее патологических состояниях, так и после рефракционных вмешательств, а также для прогнозирования риска развития кератоэктазии после операций ЛАСИК.
В настоящее время бесспорным фаворитом рефракционной хирургии является
операция ЛАСИК (LASIK). Это обусловлено быстрым и эффективным повышением
остроты зрения в результате данного вмешательства, а также комфортным
для пациента послеоперационным периодом. Современные микрокератомы и высокоточные
эксимерлазерные системы позволяют хирургам избежать многих интраоперационных
(неполный, полный срез, отверстие в центре лоскута) и послеоперационных
(гипо–, гиперкоррекция) осложнений, которые часто встречались на заре
становления вышеуказанного метода. Однако все эти осложнения, являясь
обратимыми, не представляют большой проблемы ни для пациента, ни для хирурга.
В то же время, на сегодняшний день нерешенными остаются ряд проблем, связанных с тем, что операция ЛАСИК приводит не только к уменьшению толщины роговицы, но индуцирует целый комплекс биомеханических изменений, которые не могли быть оценены каким–либо из существовавших ранее приборов. Такое осложнение операции ЛАСИК, как ятрогенная кератоэктазия или индуцированный кератоконус, встречается не так часто (0,2–0,4%), но представляет собой одну из самых серьезных проблем современной рефракционной хирургии [6, 20]. Несмотря на ряд предложенных способов приостановления прогрессирования кератоэктазии, таких как ношение специальных контактных линз [5, 8, 17], имплантация интрастромальных колец [2, 13, 19], восстановление поперечных коллагеновых связей с использованием комбинации ультрафиолетового излучения с инстилляциями рибофлавиновых капель [12, 25, 26], данное осложнение часто заканчивается сквозной пересадкой роговицы.
Одной из причин возникновения индуцированного кератоконуса является недостаточная остаточная толщина роговицы после проведенной лазерной абляции (толщина остаточного стромального ложа менее 250–270 мкм, вместе с лоскутом — менее 400 мкм), а также невыявленный при предоперационном обследовании субклинический кератоконус [20, 22]. Однако многие авторы описывают случаи развития ятрогенной кератоэктазии у пациентов с достаточной остаточной толщиной роговицы (более 450 мкм) и нормальной, не характерной для кератоконуса топографической картой [18, 23, 24]. Хотя на сегодняшний день основными скрининговыми показателями в рефракционной хирургии являются толщина роговицы и данные кератотопографии, очевидно наличие других, пока недостаточно изученных биомеханических особенностей роговичной ткани, предрасполагающих при определенных обстоятельствах (например, нарушение целостности роговицы при проведении среза) к появлению и прогрессированию ятрогенной кератоэктазии [6].
Помимо несовершенства процедуры скрининга, нерешенной остается задача точного измерения внутриглазного давления (ВГД) у пациентов, прооперированных методом ЛАСИК по поводу различных видов аметропий. Известно, что на результаты измерения ВГД всеми видами тонометров, откалиброванных по Гольдману, оказывают влияние такие свойства роговицы, как ригидность, толщина, степень гидратации, кривизна, и, возможно, ряд других, еще неидентифицированных факторов. Доказано, что после операции ЛАСИК значения ВГД по Гольдману искусственно занижаются [11, 7, 21, 1]. Однако этот факт не мог быть объяснен на основании изменения данных толщины, кривизны роговицы или других известных параметров. Противоречивые результаты специальных исследований продемонстрировали, что показатели толщины и кривизны роговицы не могут использоваться для коррекции индивидуальных значений ВГД [7, 21, 9, 3]. Предпринимаются попытки создания новых методов точного измерения ВГД у пациентов после операции ЛАСИК — это dynamic contour tonometry DCT (динамическая графическая тонометрия) [7, 11] и pressure phosphene tonometer (транспальпебральная фосфен–тонометрия) [4, 16].
Таким образом, до настоящего времени изучение in vivo биомеханических свойств роговичной ткани, а также точное измерение ВГД, независимое от изменения индивидуальных свойств роговицы, было невозможно. В научных исследованиях и на практике офтальмологи ограничивались лишь определением таких простых показателей, как толщина и топография роговицы. Для решения вышеназванных задач компанией Reichert (США) был создан новый прибор ORA — Ocular Response Analyzer, позволяющий измерить биомеханические свойства роговицы и ВГД, используя динамический двунаправленный процесс аппланации роговицы. Прибор позволяет получить данные о ВГД, сопоставить их с результатами измерения по Гольдману и оценить новый параметр, названный корнеальным гистерезисом (КГ), характеризующий вязкое затухание в роговичной ткани или, другими словами, способность ткани абсорбировать и рассеивать энергию.
В качестве внешнего воздействия в Ocular Response Analyzer используется быстрый воздушный импульс, мониторинг деформации роговицы осуществляется специальной электронно–оптической системой. Установочные процедуры автоматизированы. Точно дозированное воздействие воздушной струи заставляет роговицу двигаться назад, уплощаясь и затем незначительно прогибаясь кзади. Продолжительность воздействия составляет несколько миллисекунд, после чего давление снижается до исходного уровня, и роговица приобретает обычную конфигурацию. При этом она снова проходит через положение уплощения.
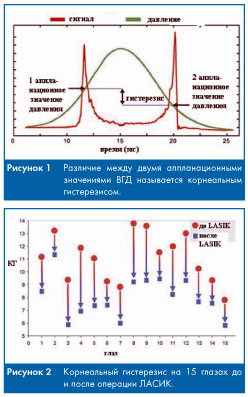
Электронно–оптическая детекторная система проводит мониторинг изменения кривизны роговицы в центральной зоне, регистрируя два независимых аппланационных значения давления: при первом уплощении роговицы, двигающейся кзади, и при втором уплощении роговицы, возвращающейся к исходной конфигурации. На первый взгляд, эти два значения давления должны быть идентичны. Однако, благодаря вязкому затуханию динамичного воздушного импульса в роговичной ткани, происходит некоторая задержка уплощения роговицы, что приводит к регистрации двух различных значений давления.
Среднее значение из этих двух показателей давления соответствует показателю ВГД по Гольдману. А разность между этими показателями является корнеальным гистерезисом и измеряется в мм рт.ст. (рис. 1). Перед проведением специальных клинических исследований КГ был измерен на 339 здоровых глазах. В здоровых глазах показатель КГ колебался от 7,73 до 18,01 мм рт.ст., составляя в среднем 12,36 мм рт.ст. [15]. Было выявлено, что величина гистерезиса остается постоянной при повторных измерениях у одного и того же человека, но значительно отличается у разных людей. Кроме того, было замечено, что значение КГ на правом и левом глазах у одного человека имеют высокую степень соответствия (R2=0.60), что свидетельствует о том, что гистерезис является детерминированным биологическим свойством организма [14, 15].
Не обнаружена связь между КГ и радиусом роговицы, степенью астигматизма, остротой зрения, длиной передне–задней оси глаза [15]. Это привело к убеждению, что КГ действительно является новым параметром, характеризующим биомеханические свойства роговицы. Кроме того, КГ измерялся при трех различных уровнях давления, искусственно создаваемых с помощью офтальмодинамометра на 32 глазах здоровых людей. Для каждого уровня ВГД значения двух аппланационных измерений сопоставлялись с результатами тонометрии по Гольдману. Результаты ясно показали, что уровень КГ остается относительно постоянным при различных уровнях ВГД, что демонстрирует независимость этого показателя от ВГД в здоровых глазах [14]. Кроме показателя гистерезиса, двойное аппланационное измерение позволяет получить дополнительную важную информацию, заключенную в понятиях роговично–компенсированного ВГД и фактора резистентности роговицы (ФРР). Оба этих параметра вычисляются с помощью специальных алгоритмов. ФРР представляет собой кумулятивный эффект эластичного и вязкого сопротивления, оказываемого деформируемой поверхностью роговицы при воздействии воздушной струи и является показателем общей резистентности роговицы. Хотя КГ и ФРР взаимосвязаны, в некоторых случаях они значительно различаются, предоставляя исследователю определенную информацию о роговице. Значение ФРР увеличивается при повышенных значениях давления по Гольдману и достоверно коррелирует с показателями толщины роговицы.
 Роговично–компенсированное
ВГД — это значение давления, рассчитанное с учетом данных о биомеханических
свойствах роговицы. Доказано, что этот показатель практически не зависит
от толщины роговицы. Собственные исследования компании Reichert продемонстрировали,
что роговично–компенсированное ВГД в гораздо большей степени отражает
реальные цифры давления по сравнению с результатами измерения по Гольдману
[10].
Роговично–компенсированное
ВГД — это значение давления, рассчитанное с учетом данных о биомеханических
свойствах роговицы. Доказано, что этот показатель практически не зависит
от толщины роговицы. Собственные исследования компании Reichert продемонстрировали,
что роговично–компенсированное ВГД в гораздо большей степени отражает
реальные цифры давления по сравнению с результатами измерения по Гольдману
[10].
Таким образом, Ocular Response Analyzer позволяет получить данные о трех новых параметрах. Хотя этот комплекс показателей полностью не изучен, его большое клиническое значение не вызывает сомнения. Клинические исследования, проведенные в течение последних трех лет, доказали, что КГ является функцией свойств роговицы, а не артефактом каких–либо других переменных. Стало очевидным, что КГ, отражающий биомеханические свойства роговицы, представляет интерес при оценке результатов различных офтальмологических исследований, а также при изучении ряда патологических состояний глаза. Кроме того, измерение КГ дает ключ к пониманию влияния биомеханических свойств роговицы на процесс измерения ВГД.
Результаты исследований продемонстрировали значительное понижение величины КГ и ФРР при заболеваниях роговицы по сравнению с показателями здоровых людей. При кератоконусе уровень КГ равнялся в среднем 8,74 мм рт.ст. (4,80–12,39 мм рт.ст.). Самый низкий показатель гистерезиса наблюдался в группе пациентов с дистрофией Фукса, несмотря на имеющееся при этом заболевании утолщение роговицы вследствие ее повышенной гидратации. Показатель КГ составил при этом заболевании в среднем 8,41 мм рт.ст. (3,60–10,37 мм рт.ст.). Низкие значения КГ присущи роговицам с меньшей способностью поглощать энергию воздушного импульса. Показатели ФРР в этих группах пациентов оказались также снижены, свидетельствуя об уменьшении по сравнению с нормой резистентности роговицы. Снижение значений ФРР при кератоконусе и дистрофии Фукса объясняют необычно низкие показатели ВГД при измерении по Гольдману на таких глазах [14, 15]. Кроме того, у пациентов с заболеваниями роговицы отмечались значительные изменения формы волновых сигналов [15].
 По
сравнению с показателями здоровых людей в группе пациентов с глаукомой
среднее значение КГ оказалось значительно сниженным, а разброс показателей
шире. Клинические исследования с использованием Ocular Response Analyzer
показали, что низкое значение КГ является независимым фактором возникновения
и прогрессирования глаукоматозного процесса [14, 15].
По
сравнению с показателями здоровых людей в группе пациентов с глаукомой
среднее значение КГ оказалось значительно сниженным, а разброс показателей
шире. Клинические исследования с использованием Ocular Response Analyzer
показали, что низкое значение КГ является независимым фактором возникновения
и прогрессирования глаукоматозного процесса [14, 15].
Значимость показателей КГ и ФРР в рефракционной хирургии не вызывает сомнения. Показатели КГ и ФРР дают более полную характеристику свойств роговицы, чем ее толщина, и достоверно различаются у людей с нормальной и патологически измененной роговицей. Тот факт, что эти показатели лишь слабо коррелируют с данными толщины роговицы, дает основание полагать, что измерение КГ в большей степени способствует выявлению пациентов с высоким риском развития эктазии после ЛАСИК. По мнению многих специалистов, пациенты с низким значением КГ и ФРР, или «мягкой» роговицей, имеют высокий риск развития послеоперационных осложнений в виде ятрогенной кератоэктазии [15]. В настоящее время в этой области проводится ряд клинических исследований.
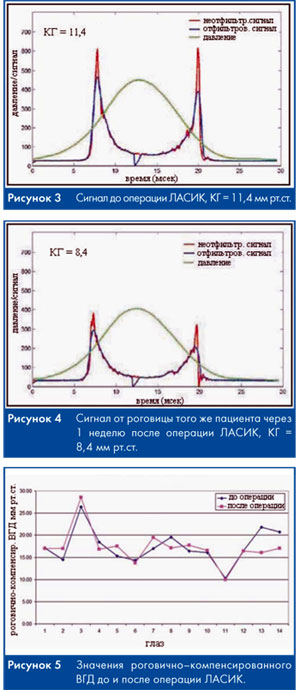
Предварительные результаты показали, что снижение значений КГ и ФРР является универсальной реакцией роговицы после операции ЛАСИК. Данные КГ до и после операции ЛАСИК представлены на рисунке 2. По мнению многих исследователей, снижение КГ и ФРР в первую очередь определяется не уменьшением толщины роговицы, а изменением ее структуры при формировании ламеллярного лоскута с последующей абляцией глублежащих слоев стромы [15]. Форма сигнала после ЛАСИК оказалась сходной с показателями при кератоконусе, что указывает на снижение в обоих случаях вязко–эластичных свойств роговицы. Кроме того, все роговицы после операции ЛАСИК демонстрировали значительно сниженный сигнал широкой амплитуды, что, возможно, указывает на увеличение локальной деформации роговицы (рис. 3, 4).
Таким образом, результаты измерения КГ имеют исключительное значение для улучшения возможностей прогноза операции ЛАСИК во время скрининга пациентов и контроля над результатами вмешательства. Кроме изложенного, по мнению ряда исследователей, измерение КГ может быть полезно при выборе алгоритма персонализированной абляции. Сегодня проводятся исследования для подтверждения этой гипотезы.
Ocular Response Analyzer позволяет получить значение роговично–компенсированного
ВГД с учетом свойств данной роговицы. Это значительно упрощает измерение
ВГД после операции ЛАСИК. Исследования показали, что Ocular Response Analyzer
демонстрирует приблизительно одинаковые результаты тонометрии на одном
глазу до и после операции (рис. 5). В то время как значения ВГД по Гольдману
после операции ЛАСИК снижаются на 2–6 мм рт.ст., уменьшение роговично–компенсированного
ВГД составляет в среднем менее 1 мм рт.ст. [10, 15].
Таким образом, Ocular Response Analyzer существенно облегчает контроль
ВГД у пациентов после операции ЛАСИК.
ЗАКЛЮЧЕНИЕ
Динамический двунаправленный процесс аппланации роговицы, используемый в Ocular Response Analyzer, позволяет измерить корнеальный гистерезис. Корнеальный гистерезис является отражением вязкого затухания в ткани роговицы и позволяет рассчитать фактор резистентности роговицы, который, в свою очередь, показывает степень общей резистентности роговицы. Оба показателя биомеханических свойств роговицы впервые введены в клиническую практику. Ряд клинических исследований доказал информативность новых параметров при прогнозировании результатов операции ЛАСИК, а также диагностике различных заболеваний роговицы.
Возможность оценить биомеханические свойства роговицы позволяет прибору рассчитать уровень роговично–компенсированного ВГД, в значительно меньшей степени зависящий от свойств роговицы, чем при других методах тонометрии. Значение роговично–компенсированного ВГД не зависит от толщины роговицы и остается неизменным после операции ЛАСИК.
ЛИТЕРАТУРА
1. Agudelo L.M, Molina C.A., Alvarez D.L. Changes in intraocular pressure
after laser in situ keratomileusis for myopia, hyperopia, and astigmatism.
J. Refract. Surg. 2002; 18(4): 472–474.
2. Alio J., Salem T., Artola A., Osman A. Intracorneal rings to correct
corneal ectasia after laser in situ keratomileusis. J. Cataract Refract.
Surg. 2002; 28(9): 1568–1574.
3. Bayraktar S., Bayraktar Z. Central corneal thickness and intraocular
pressure relationship in eyes with and without previous LASIK: comparison
of Goldmann applanation tonometer with pneumatonometer. Eur. J. Ophthalmol.
2005; 15(1): 81–88.
4. Cheng A.C., Leung D.Y., Cheung E.Y., Fan D.S., Law R.W., Lam D.S. Intraocular
pressure measurement in patients with previous LASIK surgery using pressure
phosphene tonometer. Clin. Experiment.Ophthalmol. 2005; 33(2): 153–157.
5. Choi H.J., Kim M,K., Lee J.L. Optimization of contact lens fitting in
keratectasia patients after laser in situ keratomileusis. J. Cataract Refract.
Surg. 2004; 30(5): 1057–1066.
6. Comaish I.F., Lawless M.A. Progressive post–LASIK keratectasia: biomechanical
instability or chronic disease process? J.Сataract Refract. Surg. 2002;
28(12): 2206–2213.
7. Duba I., Wirthlin A.C. Dynamic contour tonometry for post–LASIK intraocular
pressure measurements. Klin–Monatsbl–Augenheilkd. 2004; 221(5): 347–350.
8. Fernandez–Velazquez F.J. Management of a post–ELLKAT keratectasia with
a gas permeable contact lens. Clin. Exp.Optom. 2005; 88(3): 181–185.
9. Hsu S.Y., Hsu Y.C., Tsai R.K., Lin C.P. Intraocular pressure change after
laser in situ keratomileusis (LASIK). Kaohsiung J. Med. Sci. 2005; 21(4):
149–152.
10. Karmel M. New Tonometry — The Search for True IOP. EyeNet.May 2005.
— http://www.aao.org/news/eyenet/200505/
11. Kaufmann C., Bachmann L.M., Thiel M.A. Intraocular pressure measurements
using dynamic contour tonometry after laser in situ keratomileusis. Invest.
Ophthalmol.Vis. Sci. 2003; 44(9): 3790–3794.
12. Kohlhaas M., Spoerl E., Speck A., Schilde T., Sandner D., Pilluna E.
Eine neue Behandlung der Keratektasie nach LASIK durch Kollagenvernetzung
mit Riboflavin/UVA–Licht. [A new treatment of keratectasia after LASIK by
using collagen with riboflavin/UVA light cross–linking]. Klin. Monatsbl.
Augenheilkd. 2005; 222(5): 430–436.
13. Lovisolo C.F., Fleming J.F. Intracorneal ring segments for iatrogenic
keratectasia after laser in situ keratomileusis or photorefractive keratectomy.
J. Refract. Surg. 2002; 18(5): 535–541.
14. Luce D.A. Determining in vivo biomechanical properties of the cornea
with an ocular response analyzer. J. Cataract. Refract. Surg. 2005; 31(1):
156–162.
15. Luce D.A. Taylor D. Reichert Ocular Response Analyzer Measures Corneal
Biomechanical Properties and IOP. Provides New Indicators for Corneal Specialties
and Glaucoma Management. Reichert Ophthalmic Instruments. 2005, 12р.
16. Naruse S., Mori K., Kojo M., Hieda O., Kinoshita S. Evaluation of intraocular
pressure change after laser in situ keratomileusis using the pressure phosphene
tonometer. J. Cataract Refract.Surg. 2004; 30(2): 390–397.
17. O’donnell C., Welham L., Doyle S. Contact lens management of keratectasia
after laser in situ keratomileusis for myopia. Eye Contact Lens. 2004; 30(3):
144–146.
18. Ou R.J., Shaw E.L, Glasgow B.J. Keratectasia after laser in situ keratomileusis
(LASIK): evaluation of the calculated residual stromal bed thickness. Am.
J. Оphthalmol. 2002; 134(5): 771–773.
19. Pokroy,–R; Levinger,–S; Hirsh,–A Single Intacs segment for post–laser
in situ keratomileusis keratectasia. J. Cataract Refract. Surg.; 30(8):
1685–1695.
20. Rad A.S., Jabbarvand M., Saifi. N. Progressive keratectasia after laser
in situ keratomileusis. J. Refract. Surg. 2004; 20(5 Suppl): S718–22.
21. Ruangvaravate N., Thuangtong A., Kosrirukvongs P., Prabhasawat P., Booranapong
W., Srivannaboon S. Tonometry after laser in situ keratomileusis treatment:
a preliminary study in Thai patients. J. Med. Assoc. Thai. 2005; 88(3):
340–344.
22. Sekundo W., Bonicke K., Mattausch P., Wiegand W. Six–year follow–up
of laser in situ keratomileusis for moderate and extreme myopia using a
first–generation excimer laser and microkeratome. J. Cataract Refract. Surg.
2003; 29(6): 1152–1158.
23. Spadea L., Palmieri G., Mosca L., Fasciani R., Balestrazzi E. Latrogenic
keratectasia following laser in situ keratomileusis. J. Refract. Surg. 2002;
18(4): 475–480.
24. Wang J.C., Hufnagel T.J., Buxton D.F. Bilateral keratectasia after unilateral
laser in situ keratomileusis: a retrospective diagnosis of ectatic corneal
disorder. J. Cataract Refract. Surg. 2003; 29(10): 2015–2018.
25. Wollensak G., Spoerl E., Seiler T. Riboflavin/ultraviolet–a–induced
collagen crosslinking for the treatment of keratoconus. Am. J. Ophthalmol.
2003; 135(5): 620–627.
26. Wollensak G., Sporl E., Seiler T. Behandlung von Keratokonus durch Kollagenvernetzung.
Ophthalmologe 2003; 100(1): 44–49.
A B S T R A C T
Modern potentialities in prevention of post–LASIK complications
and accurate post–LASIK IOP measurement V.V.Neroev, A.T. Khanjian, O.V.
Zaitseva, Moscow Helmholtz Institute of Eye Diseases, Moscow, Russia
The Reichert Ocular Response Analyzer is the new device that utilizes a
dynamic bi–directional applanation process to measure the biomechanical
properties of the cornea and Intraocular Pressure of the eye. It provides
the assessing of the new corneal properties functions: Corneal Hysteresis
and Corneal Resistance Factor, and the calculating of Corneal–compensated
IOP that is less affected by corneal properties. The results of the clinical
studies suggest these new parameters may be clinically useful in a variety
of important areas including screening potential LASIK candi' dates for
prevention of post–surgical complications, such as corneal ectasia, and
accurate post–LASIK IOP measurement.



 Список статей
Список статей
